


Se trata de un antes y un después para la investigación neurológica, especialmente para enfermedades neurodegenerativas como el Alzheimer.
El paso que dio un equipo transdisciplinar de científicos argentinos fue decisivo al lograr en un modelo humano -no animal que supone una limitación a la hora de extrapolar los resultados a humanos- un avance sobre Alzheimer, a partir de muestras de un paciente portador de la primera mutación descripta y asociada a una familia argentina con historia de enfermedad de Alzheimer familiar (EAF) o hereditario.
Por medio de diversos experimentos, el equipo obtuvo un modelo neuronal derivado de células madre pluripotentes inducidas (iPSC) y comprobó en ellas la existencia de alteraciones en la absorción de calcio y un mal funcionamiento de las mitocondrias, lo que sugiere que estos mecanismos tienen un rol importante en la disfunción que lleva a la muerte neuronal característica de la enfermedad.
El objetivo del grupo de investigación argentino era indagar sobre las bases moleculares de la neurodegeneración en un modelo neuronal propio obtenido a partir de células de la piel de un paciente argentino.
Por primera vez en Argentina, los científicos lograron crear neuronas humanas en el laboratorio. Y, sin respiro, estas neuronas permitieron observar directamente, en un modelo real y personalizado, cómo ocurren los daños en el cerebro y qué mecanismos celulares están involucrados en el desarrollo de la enfermedad, algo que antes solo podía estudiarse en animales o de manera indirecta.
El modelo fue generado en colaboración entre el Centro de Investigación en Medicina Traslacional Severo R. Amuchástegui (CIMETSA), de Córdoba-CONICET, la Fundación Instituto Leloir y la Facultad de Medicina de la UBA, y permitió explorar en detalle los mecanismos celulares específicos implicados en la neurodegeneración.
Este avance, que ya fue publicado en la revista Scientific Reports, se basa en la obtención de células madre pluripotentes inducidas (iPSC) a partir de células de piel de un paciente argentino con Alzheimer hereditario.
El Alzheimer hereditario es una forma poco frecuente de la enfermedad, que se transmite de padres a hijos y suele manifestarse a edades más tempranas.
En la mesada del laboratorio de los científicos argentinos se lograron desarrollar neuronas humanas derivadas de células madre, a partir de un paciente portador de la mutación M146L en la Presenilina-1, vinculada al Alzheimer familiar y/o hereditario.
Las células madre pluripotentes inducidas, conocidas como iPSC, son células que los científicos pueden “reprogramar” en el laboratorio para que se conviertan en cualquier tipo de célula del cuerpo, como neuronas.
Los investigadores Carlos Wilson y Alfredo Cáceres llevaron adelante el estudio desde el CIMETSA, de Córdoba. Además, Luis Ignacio Brusco y Laura Morelli participaron del estudio desde la Facultad de Medicina de la Universidad de Buenos Aires y la Fundación Instituto Leloir, respectivamente.
En diálogo con Infobae, el doctor Brusco, decano de la Facultad de Ciencias Médicas de la UBA, director del Centro de Alzheimer del Hospital de Clínicas de la UBA y presidente de Alzheimer Argentina, explicó que “poder trabajar con neuronas obtenidas a partir de células de un paciente (con Alzheimer hereditario) permite observar en detalle cómo se desencadenan los daños en el cerebro y, a futuro, pensar en tratamientos hechos a medida para cada persona".
El especialista destacó que este avance marca un cambio de paradigma y acerca a la ciencia a herramientas concretas para profundizar la investigación sobre el Alzheimer.
En una entrevista previa con Infobae, Brusco describió: “La enfermedad de Alzheimer puede definirse como un envejecimiento acelerado del cerebro que desarticula la relación entre el tiempo mental y el corporal. Inicialmente afecta las funciones cognitivas, en especial la memoria reciente y la conducta en general”.
“Con el tiempo, compromete el sistema nervioso central en su totalidad, alterando funciones motoras, sensoriales, autónomas y los ritmos biológicos, lo que conduce a una progresiva pérdida de autonomía. Su desarrollo, que puede extenderse entre diez y quince años, presenta síntomas heterogéneos cuya manifestación varía según el individuo y su contexto”, definió el experto.
Las células madre pluripotentes inducidas, conocidas como iPSC, fueron transformadas en neuronas corticales humanas en laboratorio, lo que permitió a los investigadores observar alteraciones en la regulación del calcio y disfunción mitocondrial —las “usinas energéticas” celulares— dentro de las propias células del paciente.
El calcio y las mitocondrias cumplen funciones vitales en las neuronas: el calcio participa en la transmisión de señales, mientras que las mitocondrias funcionan como las “baterías” de la célula, suministrando la energía necesaria para su funcionamiento.
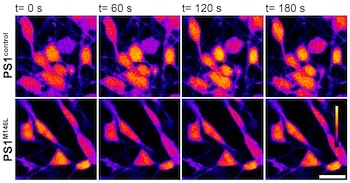
Imágenes representativas de la captación de calcio en las neuronas “control” (arr.) y en aquellas que presentan la mutación PS1 M146L (abajo) en el tiempo: de 0 a 180 segundos
Los resultados sugieren que el daño neuronal característico de la enfermedad podría estar vinculado a estos procesos y no únicamente a la acumulación de proteína beta amiloide, como se suele creer tradicionalmente.
La generación de neuronas humanas a partir de iPSC permite analizar los mecanismos de neurodegeneración en un contexto directamente relevante para la patología y abre la puerta a terapias más precisas.
Según la investigadora Laura Morelli, “estas neuronas creadas en el laboratorio reflejan mejor la fisiología del cerebro y las alteraciones específicas del paciente, facilitando el estudio de la patología y el eventual desarrollo de terapias más precisas”.
Hasta el momento, no existían antecedentes del estudio de la mutación M146L en neuronas humanas, lo que convierte este trabajo en un hito para la investigación argentina.
El análisis demostró que las neuronas portadoras de la mutación presentan una dinámica anormal del calcio, mal funcionamiento mitocondrial y mayor producción de especies reactivas de oxígeno, generando procesos inflamatorios crónicos. Carlos Wilson, primer autor del artículo, explicó que el “estado de alto metabolismo” de estas neuronas podría acelerar la muerte celular mucho antes de que las células realmente se queden sin energía.
Además, el estudio identificó que el defecto no reside en el receptor más habitual para la captación de calcio, sino en vías alternativas asociadas a los “microdominios de asociación de membranas”, los puntos de contacto entre el retículo endoplásmico y la mitocondria donde se regula el intercambio de calcio.
La utilización de neuronas humanas derivadas de iPSC permite analizar procesos patológicos en el tejido afectado, una estrategia que hasta ahora no era posible en este tipo de enfermedades.
El Alzheimer familiar representa menos del 1% de los casos, pero la relación causa-efecto es más directa, lo que facilita el análisis de los mecanismos subyacentes y la búsqueda de opciones terapéuticas específicas.
La relevancia clínica de este avance radica en que, aunque los resultados no pueden trasladarse directamente al Alzheimer esporádico, ambos tipos de la enfermedad comparten la disfunción mitocondrial y el déficit bioenergético cerebral, abriendo la posibilidad de estrategias comunes para su abordaje.
El equipo de investigación, coordinado por Alfredo Cáceres, Laura Morelli y Luis Ignacio Brusco, continuará caracterizando las rutas moleculares alteradas y evaluando el efecto de distintos fármacos sobre las alteraciones detectadas. Además, el sistema se ampliará a más pacientes y otras mutaciones genéticas asociadas al Alzheimer.
El estudio fue liderado por equipos del CIMETSA-CONICET, la Fundación Instituto Leloir y la Facultad de Medicina de la Universidad de Buenos Aires. Participaron también Carlos Wilson, Eduardo Castaño, Pablo Galeano, Gisela Novack, Lorenzo Campanelli, Andrés H. Rossi, Esteban Miglietta, María Mónica Remedi, Laura Gastaldi y Natividad Olivar.
Este trabajo marca un punto de inflexión en la investigación de enfermedades neurodegenerativas en Argentina y refuerza la importancia de los modelos celulares personalizados para el futuro de la medicina de precisión.







